2nd Batx Quim. ARTICLE 7. TEMA 6. EQUILIBRI QUÍMIC.
TEMA 6
EQUILIBRI QUÍMIC.
EQUILIBRI QUÍMIC
- REPÀS:
+ Abans dabordar lestudi de lequilibri de les reaccions químiques,
necessitem revisar alguns continguts que convé repassar :
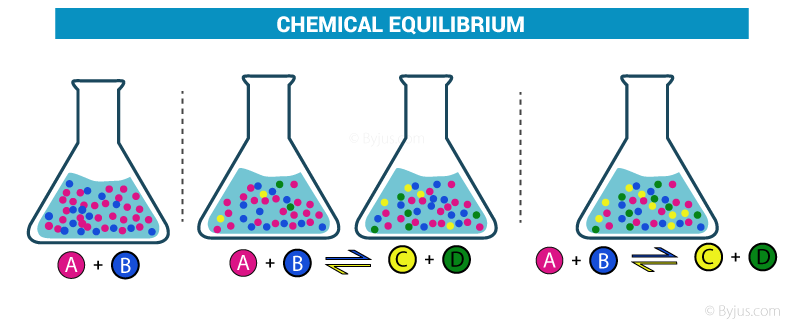
* Què és lequilibri químic : LINK (diap 2)
Aquí tens 3 vídeos on sexplica molt bé el propósit daquest tema i els conceptes inicials
que cal tenir clar abans de afrontar la resolució de problemes:
- LES CONSTANTS DEQUILIBRI Kc i Kp. FACTORS EN LEQUILIBRI :
* Diferents valors de concentracions inicials i en lequilibri per entendre el
valor de la cte en lequilibri i el significat daquest (pàg 140) : LINK
* Influència dels coeficients estequiomètrics en el valor de la Kc quan ajustem
una reacció (pàg 140) : LINK
* Influència de lordre que prenem dels membres de la reacció en el resultat
del càlcul de la constant dequilibri Kc (pàg 141) : LINK
* Exemples de valors de Kc i entendre el seu significat en diverses reaccions
químiques (pàg 141) : LINK
* Relació entre la Kc i Kp : LINK 1 (pàg 4) Pdf amb demostració
* Influència de les espècies sòlides i líquides en la Kc dequilibris heterogenis
(pàg 145) : LINK
+ Exemples dexercicis de càlcul de constants dequilibri Kc i Kp : LINK
* Aquí tens molts problemes resolts de ctes dequilibri per a repassar : LINK
+ Factors que afecten lequilibri químic :
* Quocient Qc i Qp de la reacció :
* Exemple de com evolucionen les quantitats en lequilibri quan es
modifiquen les concentracions durant aquest (pàg 152) : LINK
* Exemple de com evoluciona una reacció en equilibri al modificar la
pressió o el volum (pàg 155) : LINK
* Exemple de com varien els valors de la cte dequilibri amb la temperatura
en reaccioins endotèrmiques i exotèrmiques (pàg 156) : LINK
* Exemples dexercicis de aplicació del Principi de Le Chatelier : LINK
* Adició dun gas inert a lequilibri en diferents casos : Link
+ Equilibri físic : Diagrames de fases :
* Exemple del llibre de com explicar el comportament duna substància a partir
del seu diagrama de fases CO2 (pàg 161) : LINK
* Més informació de lutilitat i aplicació dun diagrama de fase CO2 (pàg 163) : LINK
* Dossier PAU enunciats exercicis diagrames de fases : enunciats
* Dossier PAU solucions exercicis diagrames de fases : solucions
* Exemple daplicació de la pressió de vapor (pàg 162) : LINK
- ACTIVITATS:
* Activitat del CO2 com a gas conservant del llibre : LINK
* Activitat dels motors trucats i emissió de NOx : LINK
+ Problemes :
* Solucions als exercicis del llibre de text : Solucions
* Aquí teniu molts més exercicis resolts dequilibri per a consultar : Exercicis
* Dossier PAU enunciats exercicis diagrames de fases : enunciats
* Dossier PAU solucions exercicis diagrames de fases : solucions
* En aquest web trobaràs exercicis dequilibri resolts de càlcul i aplicació del
coeficient de dissociació : Link
* Problema final coef dissociació i Kp : Pdf
- MATERIAL PER A REPASSAR EL TEMA :
+ Aquí als següents links pots repassar el més fonamental del tema i tota la lliçó :
0 comentarios