Tema 1 : Estructura, teoría y modelos atómicos. Tabla periodica de los elementos.
Lección 1 : Estructura, teoría y modelos atómicos.
Chemistry DL.
Estructura atómica.
1. Teoría atòmica :
+ ACTIVIDAD ( 1 ).
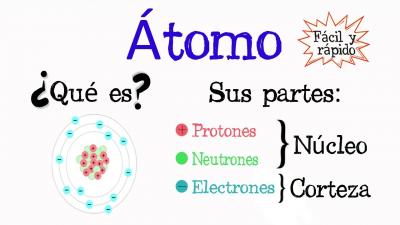
- 1a. Después de ver los videos, explica en tu libreta usando tus propias palabras que es un atomo.
- 1b. Dibuja la estructura de un átomo como este en tu libreta : atomo
* Una vez acabes, dibuja y colorea en tu cuaderno tres de los atomos
que hayas construido anteriormente.
- 2a. En grupos de 4 personas, distribuiros los diferentes modelos atómicos y, tomando
apuntes sobre uno de los modelos, explicárselos a los otros miembros del grupo.
- 2b. Por parejas, realiza un mural en una cartulina resumiendo las características principales
de cada modelo atómico.
- 2c. Actividad "Summative assessment" de evaluación sobre los modelos atómicos : Test
- 3a. Preguntas (ficha) sobre isotopos, numero atomico y masico y masa atomica :
Enunciados Solucion
- 3b. Dibuja en la libreta los esquemas de los isotopos del BERILIO de numeros masicos 8, 9 y 10.
- 3c. Actividad en grupo:
(tarjeta y explica al miembro 4)
Miembro 3 : Dibujo de los isotopos del agua : (Plantilla dibujo).
Miembro 4 : Decide cual es el dibujo mas acorde del isotopo de Potasio util para
datacion de rocas y minerales. (Plantilla dibujo).
Trabajo final de los 4 miembros del grupo (tarjeta final) :
1. Miembros 1 y 2 intercambian informacion con miembros 3 y 4,
y viceversa.
2. Despues de intercambiar la informacion entre los miembros, llegar
a una conclusion consensuada y describid la importancia de
determinados isotopos tanto para la ciencia, la industria como para la
medicina. (Tarjeta final).
- 3d. Actividad en pareja : Completar la tabla siguiente con la informacion de la pagina 72
del libro de consulta indicando otros isotopos importantes en la
vida, industria y tecnologia y su importancia y uso principal :
2. Tabla periodica de los elementos, organizacion :
+ ACTIVIDAD ( 2 ).
- Nombres de los grupos de la tabla periodica : Link
- Entendiendo la tabla periodica de los elementos : Video 1
- 1a. Escribe en la libreta los simbolos, numeros atomicos, periodos y nombre de los grupos de 3
metales, 3 semimetales, 3 no metales y 3 gases nobles.
- 1b. Usa la plantilla vacia de la tabla periodica que te da el profesor para indicar el nombre de
los diferentes grupos y familias de la tabla periodica y marca los elementos correspondien-
tes con diferentes colores : Plantilla
- Juego tarjetas tabla periodica para practicar familias y clasificacion metales : Card
> Web con imagen de los electrones de valencia, explicacion de la electronegatividad
y otras propiedades periodicas : Web
- 2a.1 Contesta a las siguientes preguntas en tu cuaderno :
> 1. Que son los electrones de la capa de valencia y que utilidad tienen?.
> 2. Dibuja en la tabla periodica vacia que te entrega el profesor los electrones de valencia
de los principales elementos de la tabla periodica segun la informacion que aparece en
la web 1 que tienes arriba indicada.
> 3. Cuantos electrones de valencia tienen los siguientes atomos y en que capa estan
situados? ( Li , Ca , Mg , Sr , Al, Cl , S , O , B , P , N , Ar )
> 4. Que relacion hay entre los electrones de valencia de un atomo y su reactividad quimica?.
* Punto 3. Reactividad de los metales : Objetivo del dia 1 , objetivo del dia 2 , objetivo del dia 3 :
* Escribe ahora en tu cuaderno la conclusion y un esquema de la tabla periodica indicando
como varia la reactividad en funcion de los electrones de valencia : conclusion
* Ahora practica con este juego de tarjetas la reactividad de algunos metales y no metales :
* Dosier de repaso de la reactividad de los elementos : Dosier Dosier solucion
Web : Cationes y aniones
* Ejercicio iones : Tabla practica iones Tabla solucion
Ejercicio : Ahora dibuja los iones correspondientes, e indica si formaran cationes o
aniones, de los atomos de : Al , Mg , O y Cl. Solucion
* Objetivo del dia : Identificacion de iones, subparticulas y reactividad.
Actividad en parejas, fichas : Instrucciones, ejemplos y tarea.
* Punto 5. - Variacion de las propiedades mas importantes de los atomos en la tabla periodica
por familias y periodos :
* Radio atomico : Objetivo del dia.
+ Con los valores de la tabla, compara los tamanos de los siguientes atomos
en una tabla de mayor a menor : tabla vacia solucion
P , Mg, Cs, Cl, Li , Co, I , Be, H , Ag, Au, Ne, Ca , O y K.
Ves al siguiente simulador y construye los atomos de H, Li, Na y K tal como
te indica el profesor y luego, sigue estas instrucciones y ordenalos por radio
atomico creciente en la tabla que te proporcionan : Instrucciones y tabla
Despues de construir y ordenar los atomos, contesta a esta pregunta:
* Energia de ionizacion : Objetivo del dia. Variacion de la EI en la tabla periodica.
* Revision de otras principales propiedades de la tabla periodica :
> Objetivo del dia : Identificar el sentido y proposito de la AE.
Afinidad electronica y electronegatividad : PDF
> En la tabla periodica que te proporciona el profesor, indica con flechas la
variacion de ambas propiedades, elctronegatividad y afinidad electronica.
> Ordena los siguientes elementos por orden creciente de electronegativdad :
O , Al, Mg , F , Fe , Cl , Na , Ne , C solucion
> Por que el F es el elemento mas electronegativo de todos y por que es mas
electronegativo que el cloro?. solucion
> Resumen pizarra de las propiedades periodicas vistas y como varian : Pic
+ ACTIVIDAD ( 3 ).
* Punto 1. Orbitales atomicos. Objetivo del dia : Definicion y caracteristicas y tipos de orbitales.
* Escribe la definicion de orbital atomico en tu libreta. Informacion orbitales.
* Observa el diagrama de la tabla periodica con los orbitales correspondientes y copiala
en la tabla vacia que te proporciona el profesor. En la parte de atras de la tabla copia
el nombre de los orbitales y su forma a partir de la siguiente imagen.
* Numeros cuanticos. Objetivo del dia : Conocer que son y su utilidad y vinculacion con
-Objetivo de dia : Relacionar orbitales y numeros cuanticos.
* Punto 2. Configuraciones electronicas: Objetivo del dia : Que son, utilidad y construccion.
2a * Video intro sobre las configuraciones electronicas : Video
2b * Video sobre las configuraciones electronicas abreviadas : Video
2d * Ejercicios de configuraciones electronicas y ejemplos :
Ex 1 soluciones Ex 2 soluciones autocorregibles en la pagina
2e * Objetivo del dia : Excepciones a las configuraciones electronicas.
Objetivo del dia : Construir excepciones de configuraciones para metales de transicion.
- ACTIVIDAD DE SINTESIS EN GRUPO (revision reactividad quimica) :
LOS GRANDES LAGOS.
Por que existen los grandes lagos? , Por que el agua se mantiene en ese lugar conservando
el agua de esos lagos en su sitio? , Como puede ser si el subsuelo de esos lagos esta
formado de sal? , Como es posible que todavia exista toda esa sal con tanta agua arriba en los lagos? , como puede ser que gracias a los lagos tengamos sal para casi toda america?
Que tiene todo esto que ver con la tabla periodica y con la reactividad de los elementos
que hemos estudiado en clase y los electrones de valencia? podrias predecir de alguna
manera y explicar lo que sucede en los grandes lagos y porque no desaparecen utilizando
lo que has aprendido en clase sobre como varia la reactividad en la tabla periodica?.
Observa este video (desde el minuto 1:27 hasta el 9:05).
Despues trabaja en grupo con 2 o 3 companeros/as mas para contestar las preguntas
anteriores realizando un informe que explique en conjunto todas ellas y proporciones una
explicacion coherente de la importancia de conocer las propiedades periodicas de la tabla
para comprender procesos naturales como este y que son la causa de que dispongamos de
tantos recursos y podamos entener donde vivimos.
informe alumnos
- 2f Objetivo del dia : Realizar el test sobre orbitales y configuraciones electronicas.
- 2g Objetivo del dia : Revision del examen sobre orbitales y configuraciones.
3. Espectroscopia :
+ ACTIVIDAD ( 1 ). Introduccion a la Espectroscopia, la luz y sus caracteristicas y aplicaciones.
* Punto 1. Objetivo del dia : La luz, como se aplica a la ciencia, que es. Introduccion a la espectroscopia.
* Punto 2. Objetivo del dia : Identificar y clasificar longitudes de onda y frecuencias del espectro visible.
* Punto 3. Objetivo del dia : Transiciones electronicas y su relacion con los especros atomicos y con las
* Punto 4. Objetivo el dia : Espectros de emision y absorcion de los elementos, significado y utilidad.
0 comentarios